Herzlich Willkommen
In Deutschland erkranken jährlich ca. 4.000 Erwachsene an einem Gliom. Wenn Sie zu den Betroffenen zählen und gerade erst die Diagnose bekommen haben, haben Sie sicherlich viele neue Informationen erhalten, die Sie erst einmal verarbeiten müssen.
Auch als Angehöriger oder Pflegender finden Sie hier viele wissenswerte Informationen.
Dieser Überblick soll Ihnen dabei helfen, die wichtigsten Dinge zu verstehen, mit denen Sie im Zusammenhang mit der
Erkrankung konfrontiert sein werden – beispielsweise wie Gliome behandelt werden. Außerdem erklärt der Leitfaden die wichtigsten der häufig genannten medizinischen Begriffe im Zusammenhang mit Gliomen.
Diese Internetseite befindet sich im Aufbau. Besuchen Sie uns gerne wieder. Mit der Zeit werden hier neue Informationen hinzugefügt werden.
Lassen Sie uns mit den Grundlagen beginnen.
Was sind Gliome?
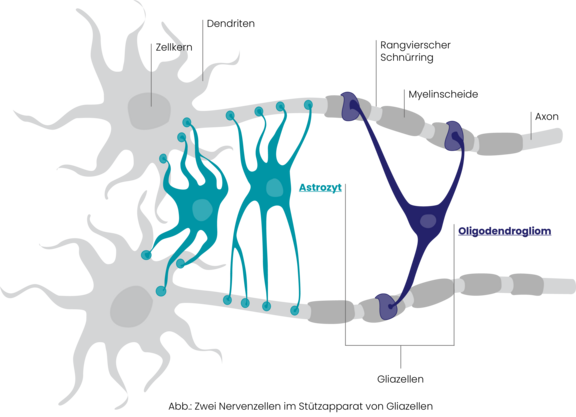
Gliome, genauer gesagt diffuse Gliome im Erwachsenenalter, sind ein Krebs, der aus bestimmten Arten von Gehirnzellen entsteht: den sogenannten Gliazellen.
Diese Zellen werden ebenfalls oft Stützzellen des Gehirns genannt. Warum das so ist, zeigt die Abbildung anhand von zwei Nervenzellen (Neurone) und einigen Gliazellen im Gehirn.
Gliome bei Erwachsenen lassen sich in drei Typen einteilen:
- Astrozytome – sie machen ~ 12 % der Gliome bei Erwachsenen aus
- Oligodendrogliome – sie machen ~ 7 % der Gliome bei Erwachsenen aus
- Glioblastome – sind mit ~ 81 % die häufigsten Gliome bei Erwachsenen
Krebszellen entstehen, wenn sich Zellen im Körper aufgrund von Veränderungen (Mutationen) im Erbgut (DNA) nicht mehr normal verhalten. Diese Zellen teilen sich unkontrolliert weiter – und das meist wesentlich schneller als gesunde Körperzellen. Daraus entsteht eine Geschwulst (Tumor), die weiterwächst. Ärzte sprechen in diesem Fall von einer bösartigen Gewebeneubildung (maligne Neoplasie).
Wie werden Gliome eingeteilt bzw. klassifiziert?
Vor 2016 wurden Gliome danach eingeteilt, wie die Zellen unter dem Mikroskop aussahen. Das konnte jedoch nicht immer eindeutig ausgewertet werden.
Aufgrund der Fortschritte im Verständnis von genetischen Veränderungen (Mutationen) hat die Weltgesundheitsorganisation (WHO) im Jahr 2021 das Klassifizierungssystem aktualisiert. Dies ermöglicht nun eine genauere Einteilung von Hirntumoren.
Heutzutage dient als Basis für die Klassifikation eine umfassende Analyse der Veränderungen in der Erbsubstanz (DNA).
Eine der wesentlichen Veränderungen der Erbsubstanz bei Gliomen im Erwachsenenalter ist die Mutation im sogenannten IDH-Gen (Isocitrat-Dehydrogenase-Gen). Diese IDH-Mutation spielt eine zentrale Rolle bei der Einteilung des Gliomtyps. Hinzu kommen weitere Veränderungen wie z. B. die sogenannte 1p/19q-Kodeletion, um den Subtyp genauer zu bestimmen.
Die WHO-Klassifikation 2021 unterteilt Gliome in drei Typen. Diese drei Typen können in unterschiedlichen Graden auftreten. Je höher der Grad, desto schneller wächst das Gliom.
IDH-Mutation – Ein früher Treiber der Gliomentstehung
IDH1- oder IDH2-Mutationen führen zu einer Anhäufung des Stoffwechselprodukts 2-Hydroxyglutarat (2-HG), welches zur Entstehung von bösartigen Tumoren führt. Dies hat vielfältige Auswirkungen auf die Gliazelle und ihre Umgebung wie u. a.
- Veränderungen der Struktur und folglich der Funktion der Erbsubstanz (epigenetische Veränderungen) oder
- eine Reduktion der T-Zellfunktion.
IDH1- oder IDH2-Mutationen führen zu einer Anhäufung des Stoffwechselprodukts 2-Hydroxyglutarat (2-HG), welches zur Entstehung von bösartigen Tumoren führt. Dies hat vielfältige Auswirkungen auf die Gliazelle und ihre Umgebung wie u. a.
- Veränderungen der Struktur und folglich der Funktion der Erbsubstanz (epigenetische Veränderungen) oder
- eine Reduktion der T-Zellfunktion.
Daher stellt die WHO-Klassifikation (2021)
die IDH-Mutation in den Mittelpunkt der Klassifikation
der Gliome bei Erwachsenen.
Daher stellt die WHO-Klassifikation (2021)
die IDH-Mutation in den Mittelpunkt der Klassifikation
der Gliome bei Erwachsenen.
IDH-Mutation –
Was bedeutet das genau?
Jede spezialisierte Zelle, so auch Gliazellen, stammen von einer Stammzelle, einer Art Ursprungszelle, ab. Stammzellen sind undifferenzierte bzw. unreife Zellen, die noch nicht auf ihre Funktion im Organismus festgelegt sind. Diese können sich durch Teilung vermehren und entwickeln (ausdifferenzieren).
Daran ist Isocitrat-Dehydrogenase (IDH), ein Stoffwechselenzym, maßgeblich beteiligt.
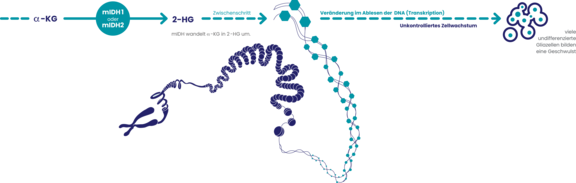
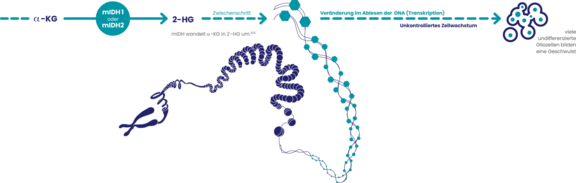
Liegt mutiertes IDH (mIDH) vor, so kann das folgenreich für die Zellteilung und das Erbgut sein: Mutiertes IDH produziert hohe Spiegel des Stoffwechselprodukts 2-HG (2-Hydroxyglutarat).
Sie bestimmen das Tumormikromilieu und haben einen erheblichen Einfluss auf das Tumorwachstum. Große Mengen 2-HG führen zu Veränderungen im Ablesen der DNA (Transkription).
Dadurch bilden sich immer mehr unreife Gliazellen, die in Verbindung mit weiteren Genmutationen (ATRX-Mutation oder 1p/19q-Kodeletion) zur Entstehung eines Astrozytoms oder Oligodendroglioms führen können.
Die IDH-Mutation ist ein zentrales Ereignis
in der Gliomentstehung.
Die IDH-Mutation ein zentrales Ereignis in der Gliomentstehung.
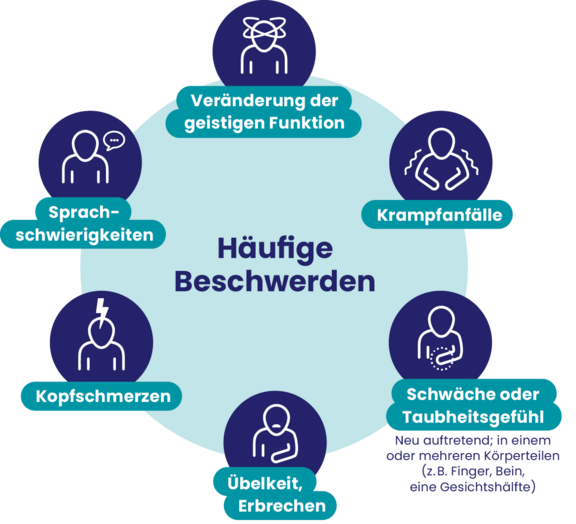
Was sind die häufigsten Symptome eines Glioms?
Gliome können die normale Gehirnfunktion beeinträchtigen und verschiedene Symptome verursachen.
Diese Beschwerden können bei manchen Patienten mild sein, während sie bei anderen starke Einschränkungen im Alltag hervorrufen. Die Symptome hängen von der Tumorart und -lokalisation ab – also der Stelle im Gehirn, an der sie liegen.
Sowohl vor als auch nach der Diagnose eines Glioms können Beschwerden auftreten.
Zusätzlich kann eine Krebsdiagnose überwältigend sein und zu psychozialer Belastung sowohl bei den Betroffenen als auch bei ihren Angehörigen führen – beispielsweise wenn es darum geht, sich um die Kinder zu kümmern, Arbeit und Ausbildung gerecht zu werden oder Sport zu treiben.
Bitte achten Sie auf alle Veränderungen,
die Ihnen auffallen. Sie können relevant für die
spätere Behandlung sein.
Bitte achten Sie auf alle Veränderungen,
die Ihnen auffallen. Sie können relevant für die
spätere Behandlung sein.
Mögliche Stationen eines Behandlungswegs
Die Behandlung eines Glioms ist individuell sehr unterschiedlich. Sie folgt jedoch bestimmten Abläufen und Prinzipien, die wir hier für Sie als Zusammenfassung dargestellt haben.
Von der OP zur Diagnose
Es klingt vielleicht überraschend, aber erst das OP-Ergebnis bringt die Diagnose – wenn auch die Bilder des Gehirn-Scans (MRT) schon wichtige Anhaltspunkte liefern.
Es sind die Ergebnisse aus der Untersuchung des entnommenen Gewebes, die die definitive Diagnose bestimmen und richtungsweisend für die Therapie sind.
Gehirn-Untersuchung:
MRT-Scan
Die Magnetresonanztomographie ist das wichtigste Verfahren zur Diagnose eines Hirntumors, denn es liefert nötige Angaben z. B. zur Lage und zum Ausmaß der Gewebeschädigung. Anhand der hochauflösenden Gehirnscans kann Ihr Behandlungsteam die Maßnahmen zur weiteren Behandlung festlegen.
In einem MRT wird ein Magnetfeld erzeugt, was es ermöglicht, daraus Bilder der Gehirnstrukturen abzuleiten.
Die Untersuchung ist schmerzfrei und belastet Sie nicht mit Strahlen.
Vorbereitung auf eine Operation
(Resektion)
Wenn Sie gemeinsam mit Ihrem Arzt die Ergebnisse Ihres Gehirn-Scans besprechen, wird er Ihnen erklären, ob bei Ihnen eine Operation durchgeführt werden kann.
Ziel dieser Operation ist es, so viel Tumorgewebe wie möglich zu entfernen. Ihr Arzt wird dies als Teil- oder Totalresektion bezeichnen. Das bedeutet, dass er versuchen wird, große Teile des Tumors (Teilresektion) oder den gesamten Tumor zu entfernen (Totalresektion). Sowohl die Größe als auch die Lage Ihres Tumors haben Einfluss darauf, ob und wie viel davon entfernt werden kann.
Diagnose
Während der Operation wird eine Probe des Tumors zur Analyse entnommen und anschließend an ein Pathologielabor geschickt. Dort wird festgestellt, um welche Art von Tumor es sich bei Ihnen handelt.
Der Bericht der Gewebeuntersuchung wird Ihnen und Ihrem Arzt helfen, den nächsten Schritt auf Ihrem Behandlungsweg zu bestimmen.

Nach der Operation
Nach der Operation dürfen Sie sich erholen, bevor Sie mit dem nächsten Teil Ihrer Behandlung beginnen. Ihr Arzt wird dann zusätzliche Tests durchführen, um die geeigneten nächsten Schritte Ihrer Therapie mit Ihnen festzulegen. Diese werden dann durch ein Team von Spezialisten begleitet.
Es bestehen mehrere Therapie-Möglichkeiten nach Ihrer ersten Operation. Ihr Behandlungsteam stellt mit Ihnen einen Plan zusammen, der individuell auf Ihre Bedürfnisse und Wünsche zugeschnitten ist.
Sprechen Sie offen über Ihre Hoffnungen, Wünsche und Sorgen,
damit Ihr Behandlungsteam diese in der weiteren Planung berücksichtigen kann.
Sprechen Sie offen über Ihre Hoffnungen, Wünsche und Sorgen, damit Ihr Behandlungsteam diese in der
weiteren Planung berücksichtigen kann.
Welche Therapie-Optionen gibt es?
Die Diagnose ist ausschlaggebend dafür, welche Möglichkeiten der Therapie für Ihre Tumorerkrankung zur Verfügung stehen.
Was erwartet Sie bei Ihrer Gliom-Behandlung? Sprechen Sie über Ihre Erwartungen! Ihr Behandlungsteam wird diese berücksichtigen, wenn es Ihren Behandlungsplan erstellt.
Ein Behandlungsplan umfasst,
- ob und wann die Behandlung beginnt,
- welche Art der Therapie für Sie geeignet ist und
- wie häufig Ihre Nachsorgetermine stattfinden.
Die folgenden Therapie-Möglichkeiten, die teilweise auch in Kombination stattfinden, stehen grundsätzlich zur Verfügung. Welche für Sie wann in Frage kommen, entscheidet Ihr Behandlungsteam zusammen mit Ihnen.
Operation (Resektion)
Häufig sind Gliome operierbar. Voraussetzung dafür ist sowohl die Größe und Lage des Tumors als auch Ihre körperliche Verfassung.
Eine Operation kann z. B.
- den Druck im Gehirn reduzieren,
- das weitere Wachstum des Glioms herauszögern und
- die Beschwerden lindern.
„Abwarten und Beobachten“
(wait and scan)
Nach der Operation trifft sich eine Expertenrunde der Gliom-Behandler (Tumorboard), die das für Sie beste Vorgehen beschließt.
Nicht immer muss nach der Gliom-OP sofort eine weitere Therapie begonnen werden. Dann ist ein Abwarten mit regelmäßigen Nachkontrollen möglich. Ihr Behandler wird mit Ihnen besprechen, ob und wann eine weitere Behandlung begonnen werden kann.
Strahlentherapie
Die Bestrahlung ist eine Art der Krebsbehandlung, bei der präzise Strahlen zur Zerstörung von Krebszellen eingesetzt werden. Nach einer OP können die möglicherweise verbliebenen Krebszellen dadurch zusätzlich angegriffen werden. Die Strahlentherapie wird oft mit einer Chemotherapie kombiniert. Den Ablauf sowie mögliche Nebenwirkungen bespricht Ihr Behandlungsteam mit Ihnen.
Chemotherapie
Eine Chemotherapie bei Gliomen kann als Infusion (Gabe in die Vene) oder als Tablette verabreicht werden. Nach einer OP können die verbliebenen Krebszellen dadurch zusätzlich behandelt werden. Sie wird oft in Kombination mit einer Strahlentherapie eingesetzt. Informationen zum Ablauf sowie möglichen Nebenwirkungen erhalten Sie von Ihrem Behandlungsteam.
Klinische Studien
Die Krebstherapie verbessert sich ständig. Daher stehen zum Zeitpunkt Ihrer Diagnose möglicherweise neue oder experimentelle Behandlungen zur Verfügung.

Diese können entweder direkt über Ihr Behandlungsteam oder über eine Teilnahme an bereits laufenden klinischen Studien erhältlich sein. Ihr Arzt kann Sie in eine dieser Studien oder Programme einschreiben, wenn das für Sie in Frage kommt.

Besprechen Sie diese Option daher mit Ihrem Arzt.
Auch die Nachsorge ist ein wichtiger Teil Ihrer Behandlung.
Und die Nachsorge?
Die Nachsorge ist als Richtungsweiser und Begleiter im Alltag unersetzbar.
Nachsorgetermine, einschließlich MRTs, sind ein wichtiger Bestandteil Ihres Behandlungsplans. Diese Termine sollen Ihnen und Ihrem Arzt dabei helfen, den Überblick über Ihre Behandlung und deren Wirksamkeit zu behalten.
Die Nachsorgetermine finden zu Beginn Ihrer Behandlung in der Regel häufiger statt und können im Laufe der Zeit seltener werden. Folgetermine sind individuell und hängen von Ihrem Behandlungsplan und Ihren möglichen Beschwerden oder Einschränkungen ab.
Je nachdem, welche Behandlung Sie erhalten haben – sei es eine Operation, Strahlentherapie oder Chemotherapie –, können Nebenwirkungen auftreten, die Ihre täglichen Aktivitäten beeinträchtigen. Sprechen Sie mit Ihrem Arzt darüber!
Zur Nachsorge gehört auch, Ihre Blutzellen und Ihre Organfunktion zu untersuchen und Sie nach
- möglichen Nebenwirkungen,
- neuen Symptomen,
- Ihrer geistigen Leistungsfähigkeit und
- Ihrem Alltag zu fragen.
Das Gliom-Expertenteam
Die Gliom-Behandlung ist eine Gemeinschaftsleistung durch verschiedene Fachärzte und Spezialisten (interdisziplinäres Team).
Dabei handelt es sich um ein individualisiertes Konzept, was sich an Ihrem Bedarf orientiert, um Ihnen die vielversprechendste Therapie und Nachsorge zukommen zu lassen.
Abhängig von Ihren Symptomen, können verschiedene Spezialisten Ihr Reha-Team verstärken.
Daher ist wichtig, dass Sie sich mitteilen und alle Ihre Fragen stellen. Nur so kann Ihnen bestmöglich geholfen werden.
Sie stehen im Zentrum eines
interdisziplinären Teams.
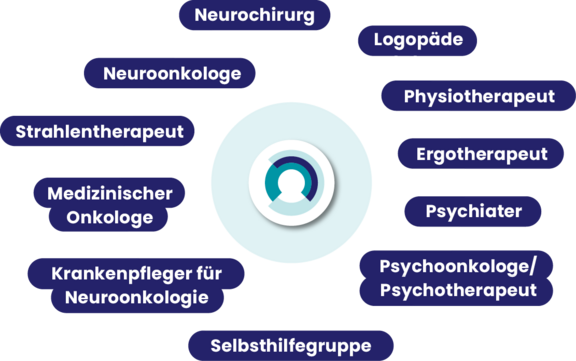
Mitglieder des interdisziplinären Gliom-Expertenteams
Mitglieder des interdisziplinären Gliom-Expertenteams
Sie stehen im Zentrum eines
interdisziplinären Teams.
Neurochirurg
Ein auf die Operation des Gehirns spezialisierter Operateur (Chirurg).
Neuroonkologe
Ein auf die Behandlung von Patienten mit Krebserkrankungen oder Tumoren des Gehirns spezialisierter Arzt.
Radioonkologe – Strahlentherapeut
Ein Arzt, der sich auf den Einsatz von Strahlung zur Behandlung von Krebs spezialisiert hat.
Medizinischer Onkologe
Ein Arzt, der auf die Behandlung von Krebspatienten spezialisiert ist.
Krankenpfleger für Neuroonkologie
Ein Krankenpfleger, der auf die Unterstützung von Patienten mit Hirntumoren fokussiert ist.
Logopäde (Sprachtherapeut)
Ein Therapeut, der mit Patienten an der Wiederherstellung und Verbesserung ihrer Sprache und Kommunikationsfähigkeiten arbeitet.
Physiotherapeut
Ein Experte für die Untersuchung, Prüfung und Behandlung körperlicher Probleme. Er setzt Handgriffe, Übungen und verschiedene Methoden ein, um die Kraft, Beweglichkeit und Funktion des Körpers wiederherzustellen oder zu erhalten.
Ergotherapeut
Ein Therapeut, der mit Patienten an funktionellen/motorischen Beeinträchtigungen arbeitet. Ziel ist die Verbesserung der für das tägliche Leben und Arbeiten erforderlichen Fähigkeiten.
Psychiater
Ein Facharzt für die psychische Gesundheit. Er kann beraten und Medikamente bei psychischen und psychosomatischen Beschwerden verschreiben.
Psychoonkologe/Psychotherapeut
Ein Experte im Bereich der psychischen Gesundheit. Sie beraten Patienten, um deren geistige und emotionale Gesundheit zu verbessern.
Selbsthilfegruppe
Diese Gruppen bieten weitere Möglichkeiten, sich zu informieren (Veranstaltungen, Austausch mit Betroffenen u. Ä.).